چون از دستگاه اسپکتروفتومتر زیرقرمز (FTIR) برای تجزیه نمونه های جامد، مایع و گاز استفاده می شود، باید برای انتقال هر یک از آنها روش مناسبی وجود داشته باشد. موضوع مشترکی که در همۀ روش های مورد تجزیه با اسپکتروفتومتر FTIR باید در نظر داشت، شفاف بودن نمونه نسبت به نور IR است، یعنی ظرفی که نمونه در آن قرار داده شده و موادی که آنالیت با آن مخلوط شده است، تابش زیرقرمز را جذب نمی کند. تعدادی از ترکیبات یونی مانند NaCl و KCl این ویژگی را دارند و لذا رایج ترین مواد برای جنس سلول ها در این طیف سنجی هستند. با توجه به دامنه طول موج مورد استفاده در اسپکتروسکوپی زیرقرمز، از مواد دیگری نیز به عنوان سلول استفاده می شود (جدول زیر).
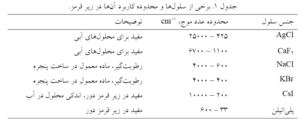
به طور کلی برای نمونه برداری از مواد جامد و رسم طیف زیرقرمز آنها چهار روش به شرح زیر وجود دارد.
- محلول کردن: در این روش نمونه جامد در حلال مناسبی حل می شود. سپس حلال خالص در سلول مایع مرجع و محلول نمونه در سلول نمونه ریخته شده و طیف زیرقرمز آن رسم می شود. این روش برای همۀ نمونه های جامد قابل استفاده نیست، زیرا تعداد حلالهای مناسب برای این عمل محدود است و یک حلال مناسب برای همۀ محدودۀ طیف زیرقرمز وجود ندارد.
- تشکیل فیلم نازک: اگر نمونه جامد بی شکل باشد، مقداری از آن در یک حلال با نقطه جوش کم حل شده و سپس مقداری از محلول روی قرص های NaCl یا KBr ریخته می شود. سپس تبخیر حلال باعث تشکیل لایه نازکی از ماده بر روی قرص می شود. مواد پلیمری را می توان با قرار دادن مقدار کمی از نمونه در بین دو سطح شیشه ای یا فلزی صیقلی و گرم کردن ملایم آنها به شکل فیلم نازک تبدیل کرد. سپس این فیلم نازک از بین سطوح جدا شده و طیف آن رسم می شود.
- روش مل: در این روش پودر کاملاً ریز شدۀ نمونه با یک روغن معدنی (به نام نوجل) مخلوط و یکنواخت می شود. سپس مقدار کمی از این خمیر شفاف در بین دو پنجره NaCl یا KBr قرار داده شده و طیف نمونه رسم می شود. اگرچه نوجل در تمام ناحیۀزیرقرمز شفاف است، ولی به دلیل داشتن جذب هایی در اعداد موج ۲۸۱۵ ،۱۴۶۲ ،۱۳۶۷و ۷۱۹ معایبی نیز دارد.
- روش تهیه قرص فشرده: در این روش مقدار بسیار کمی از نمونه کاملاً پودر شده با مقدار حدود ۱۰۰ برابر از KBr بسیار خالص در یک هاون عقیق پودر و یکنواخت می شود. سپس مقداری از آن در بین دو قطعه فلزی صیقلی که اجزایی از یک قالب مخصوص هستند، ریخته شده و تحت فشار زیاد(حداقل psi25) به شکل قرص نازکی تبدیل می شود.
این روش نسبت به روش استفاده از نوجل مزایایی دارد که عبارتند از: (الف) قرص های KBr را می توان برای مدت زیادی نگه داری کرد. (ب) غلظت آنالیت را می توان در اندازه مشخصی در قرص تنظیم و لذا از این روش در تجزیه کمی استفاده کرد. (ج) قدرت تفکیک پیک ها در قرص KBr نسبت به روش نوجل خیلی بهتر است. برای انجام مطالعات در فرکانس های کم می توان از هالیدهای قلیایی دیگر مانند CsI و CsBr استفاده کرد.
روش تهیه قرص KBr معایبی نیز دارد. (۱) به علت جذب رطوبت توسط KBr همیشه پیک مربوط به OH در عدد موج ۳۴۵۰ cm-1 مشاهده می شود،که دقت لازم برای بررسی هرگونه پیکی را در این ناحیه می طلبد. (۲) فشار زیاد ممکن است با تغییراتی در ساختار بلوری و ماهیت آنالیت همراه باشد و این موضوع به ویژه در مورد تجزیه کمپلکس های معدنی از اهمیت بیشتری برخوردار است. برای مثال، هنگام تجزیه یک نمونۀ کمپلکس با روش زیرقرمز امکان دارد که یک یا چند لیگاند موجود در آن در اثر فشاری که توسط هاون ایجاد می شود، با یون برمید موجود در KBr جایگزین شود. زیرا برمید لیگاندی قوی است و می تواند با لیگاند موجود در کمپلکس رقابت کند. (۳) این روش برای تجزیه مواد پلیمری مناسب نیست.


